Nova estratégia de farmacovigilância para medicamentos GLP-1
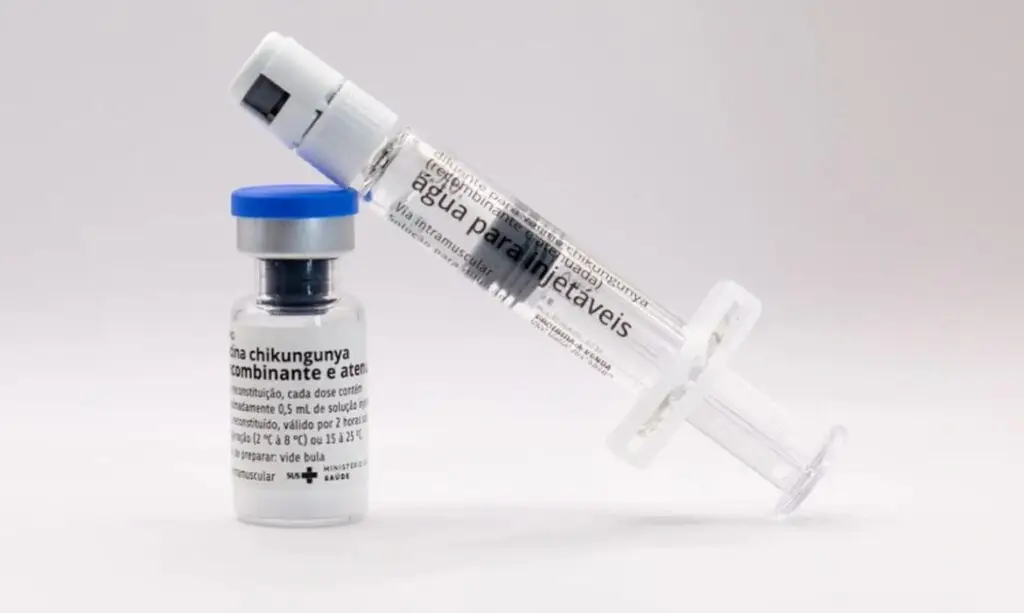
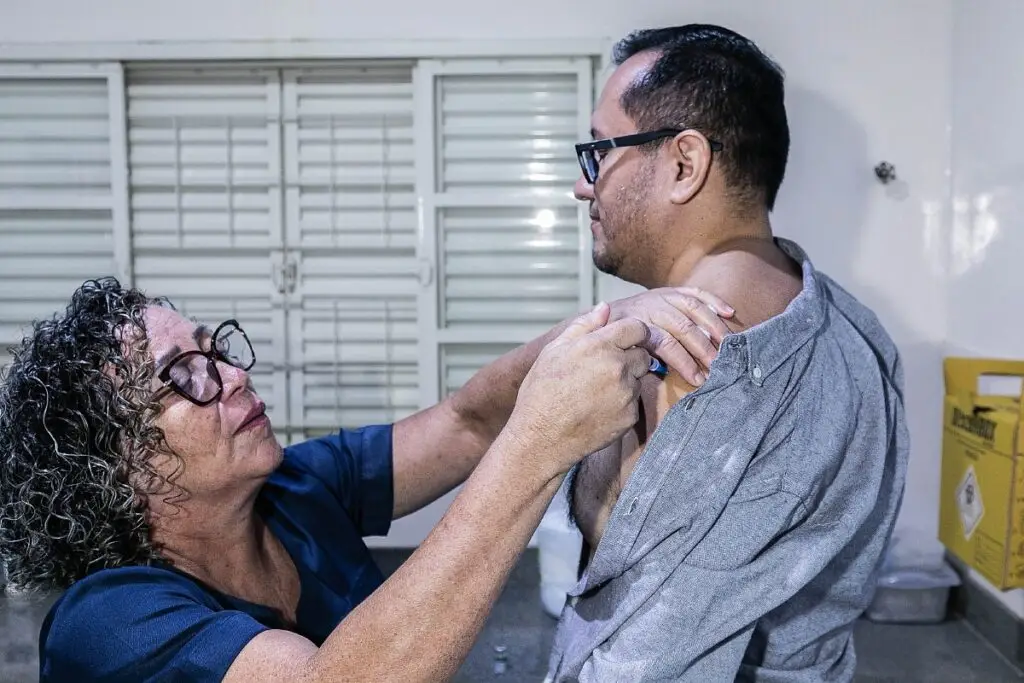
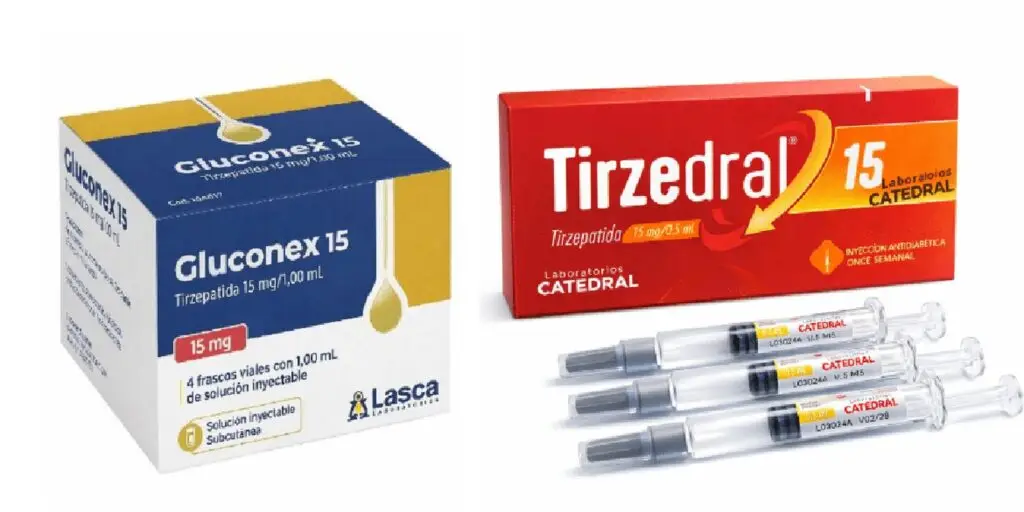
A Agência Nacional de Vigilância Sanitária (Anvisa) oficializou a implementação de um Plano de Farmacovigilância Ativa focado no uso de medicamentos agonistas do receptor do GLP-1, amplamente conhecidos como canetas emagrecedoras. A medida surge como resposta ao aumento expressivo do consumo desses fármacos no Brasil, muitas vezes utilizados para finalidades ou formas não previstas em bula.
Diferente do modelo anterior, que dependia exclusivamente de relatos voluntários, a nova estratégia estabelece um monitoramento proativo em parceria com estabelecimentos de saúde. O objetivo é identificar de forma sistemática eventuais efeitos colaterais e complicações associadas ao uso desses produtos, garantindo maior segurança aos pacientes.
Dados e riscos associados ao uso indiscriminado
Entre 2018 e março de 2026, o órgão registrou 2.965 notificações de eventos adversos relacionados a esses medicamentos. O ano de 2025 apresentou um volume expressivo de casos, com predominância de ocorrências vinculadas à semaglutida. A diretoria da agência enfatiza que, embora os fármacos possuam benefícios comprovados para o tratamento de diabetes e obesidade, a expansão do uso sem acompanhamento clínico adequado tem gerado preocupações sanitárias.
O diretor Thiago Lopes Cardoso Campos ressaltou que a alta demanda tem impulsionado a circulação de produtos falsificados ou manipulados de forma inadequada. A comercialização de itens sem garantia de origem configura crime previsto no Código Penal, expondo a população a riscos graves, como a falta de esterilidade e dosagem incorreta, que podem resultar em danos irreversíveis.
Rede de cooperação e monitoramento pós-venda
A iniciativa de vigilância conta com o suporte da Rede Sentinela, que integra hospitais universitários, laboratórios clínicos e serviços de assistência farmacêutica. A colaboração com a HU Brasil e o acordo de cooperação firmado com a Polícia Federal reforçam o combate à venda ilegal e a qualificação das notificações enviadas ao sistema de saúde.
Para o diretor-presidente da Anvisa, Leandro Safatle, a fase pós-comercialização é fundamental para detectar riscos raros ou tardios. A agência defende que a inovação farmacêutica não deve obscurecer os perigos do uso indiscriminado, exigindo uma postura firme e coordenada para proteger a saúde pública frente ao cenário atual de consumo.
Fonte: agenciabrasil.ebc.com.br